生物经济的快速增长离不开高产、稳定、具有自主知识产权的工业菌株。尽管天然工业菌株具有多样性、适应性和稳定性等优点,但它们在代谢途径、底物利用、产品得率、基因编辑工具和遗传改造方面存在挑战。因此,将非模式微生物人工改造为高效细胞工厂,对于推动生物经济的绿色、低碳和循环发展至关重要。
近日,西安交通大学教授费强团队联合湖北大学教授杨世辉团队在开发非模式微生物运动发酵单胞菌为非粮平台化合物高效生物炼制底盘方面取得重要研究进展。该研究以非模式微生物底盘细胞运动发酵单胞菌为范例,构建了酶约束的高精度全基因组代谢网络模型,提出了“主流代谢途径弱化中间底盘”工业菌株改造新策略,并以中间底盘为基础构建了D-乳酸高产稳产菌株,可以利用非粮水解液“脏糖”生产生物基乳酸,显示出良好的经济性和降低CO2排放的环保效益。该研究成功突破了运动发酵单胞菌必须生产乙醇才能生存而制约其作为非粮平台化合物生物炼制底盘的瓶颈,为其它模式与非模式微生物底盘细胞的改造提供新的改造策略和参考。相关研究成果发表于Nature Communications。
团队以具有独特优势的天然乙醇生产菌株运动发酵单胞菌(Zymomonas mobilis)为研究对象,开发了整合系统生物学信息的一站式知识数据库平台,促进对工业菌株特性的充分认识。创建了具有自主知识产权的内外源基因组编辑工具,并建立成通用基因组高效编辑工具包。克服非模式多倍体工业菌株认知少、工具缺、改造难、产物单一的痛点;建立基于运动发酵单胞菌的大宗平台化合物非粮生物炼制细胞工厂,以多元生物基原料生产多种生物燃料、生物农药、生物材料及其前体,如乙醇、乳酸、异丁醇、2,3-丁二醇、PHB等。
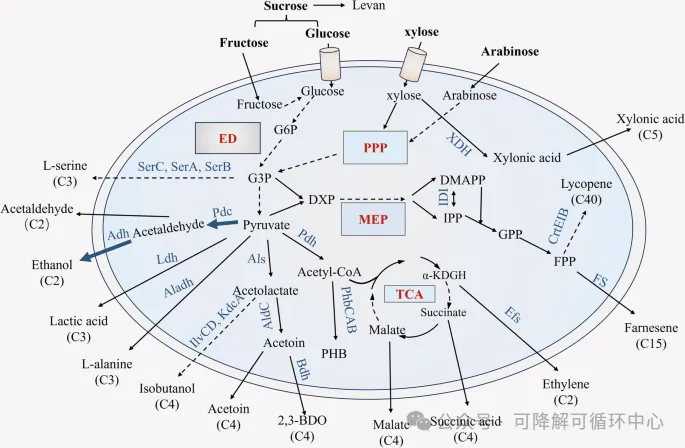
使用Z. mobilis作为底盘生产生化产品的总结
在这项工作中,通过优化全基因组代谢网络模型iZM516,并增加酶约束条件,构建了运动发酵单胞菌高精度酶约束代谢网络模型eciZM547。该模型成功指导运动发酵单胞菌C2-C5化合物的生产,实现了包括丁二酸、乙二醇、乙醇酸、1,4-丁二醇、1,3-丙二醇等系列细胞工厂的构建。为代谢途径的理性设计提供了科学指导。
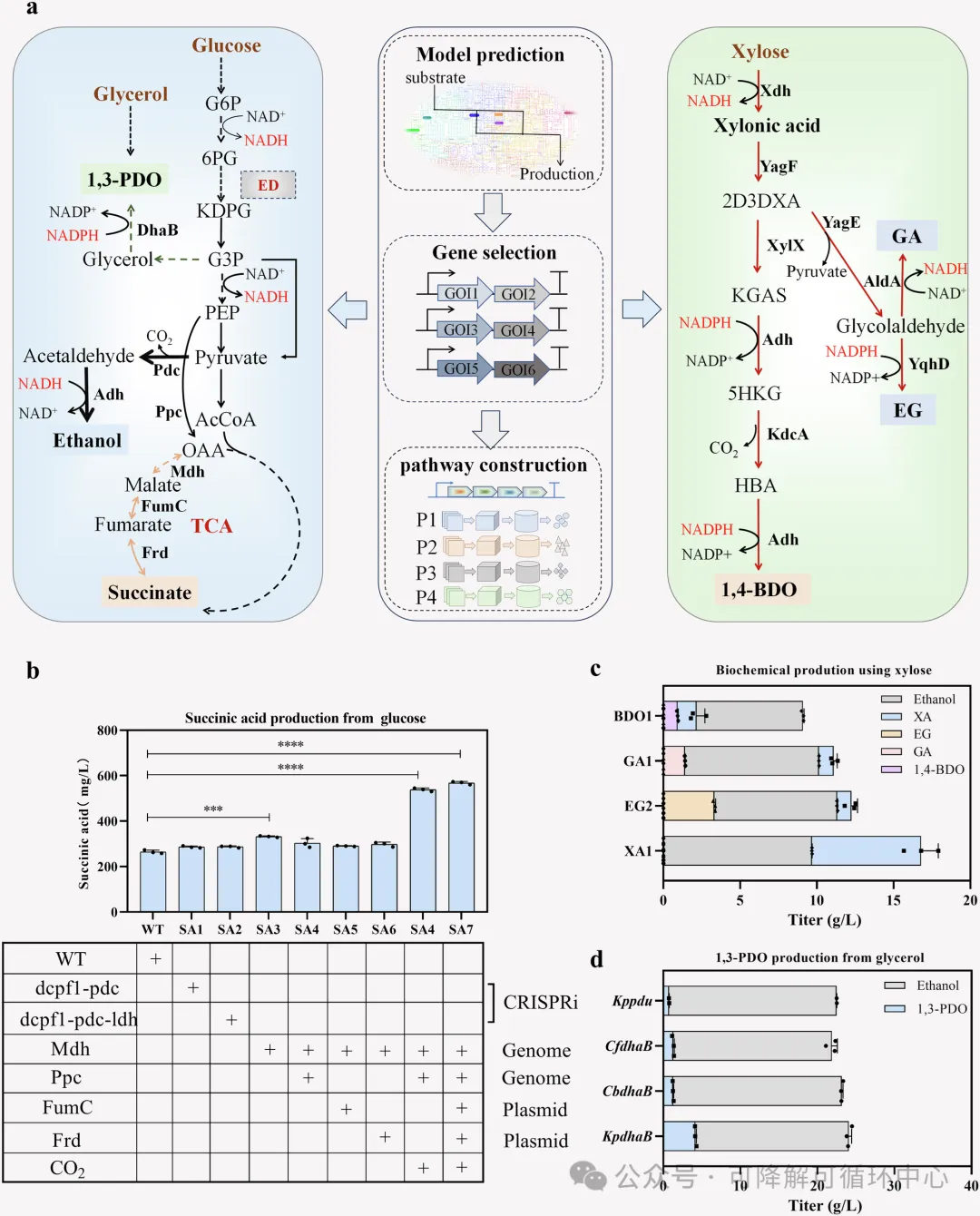
模型引导的路径设计和微生物细胞工厂的构建
研究发现,运动发酵单胞菌天然主流乙醇途径严重影响其它化合物的生产。为克服这一限制,研究者在高精度酶约束代谢网络模型指导下,开发了一种主流代谢受损的中间底盘(DMCI)策略,通过构建了低毒、辅因子不平衡的2,3-丁二醇途径(中间底盘ZMB3)来调整代谢流,从而实现了乙醇途径的完全阻断(图2)。碳代谢流结果进一步显示,几乎96%的碳源绕过主流乙醇代谢途径,用于2,3-BDO生产。
为了验证主流代谢受损的中间底盘在大宗平台化合物生产中的优势,研究人员从中间底盘ZMB3出发,构建得到乙醇途径完全阻断的D-乳酸生产重组菌株(ZMB6),该菌株可以从葡萄糖和玉米芯残渣水解液中分别生产超过140.92 g/L和104.6 g/L的D-乳酸,转化率>0.97 g/g,手性纯度高达99.9%。
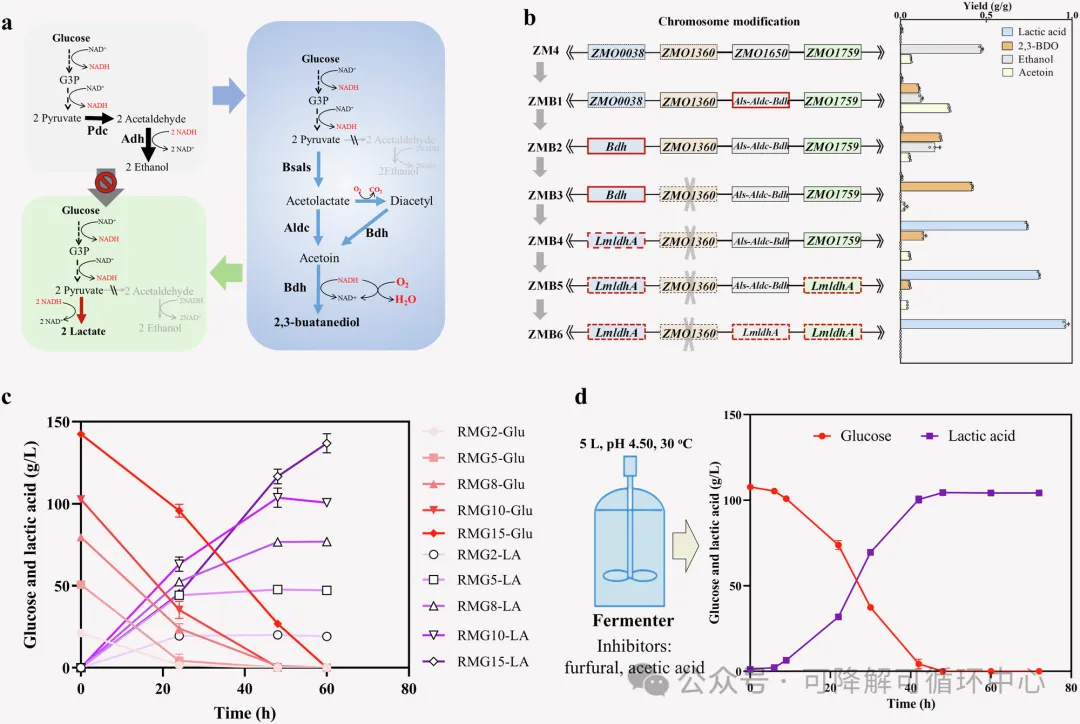
主导代谢妥协中间底盘策略的开发
通过引入2,3-BDO途径来绕过Z. mobilis的主导乙醇代谢路径,进而构建D-乳酸生产菌的策略。通过基因编辑和代谢工程,实现了从乙醇到D-乳酸生产的转变,这对于提高Z. mobilis作为生物炼制底盘的灵活性和应用范围具有重要意义。
此外,技术经济可行性分析(TEA)和全生命周期评价(LCA)证实了以木质纤维素为原料生产D-乳酸的商业潜力及CO2减排能力(图3)。TEA结果显示,D-乳酸最低售价(MSP)$ 0.28-0.45/kg,远低于以淀粉、葡萄糖、糖蜜为原料的乳酸的MSP,具备明显的竞争优势。除此之外,LCA结果则指出利用该技术生产每吨D-乳酸可减少22.51吨CO2排放量。本研究提出了主流代谢受损的中间底盘新策略用于指导大宗平台化合物底盘细胞的高效构建,构建利用非粮水解液“脏糖”高产D-乳酸的重组菌株,这项工作不仅拓宽了运动发酵单胞菌作为优良生物炼制底盘细胞的生产应用范围,也为工程化改造工业菌株提供参考。
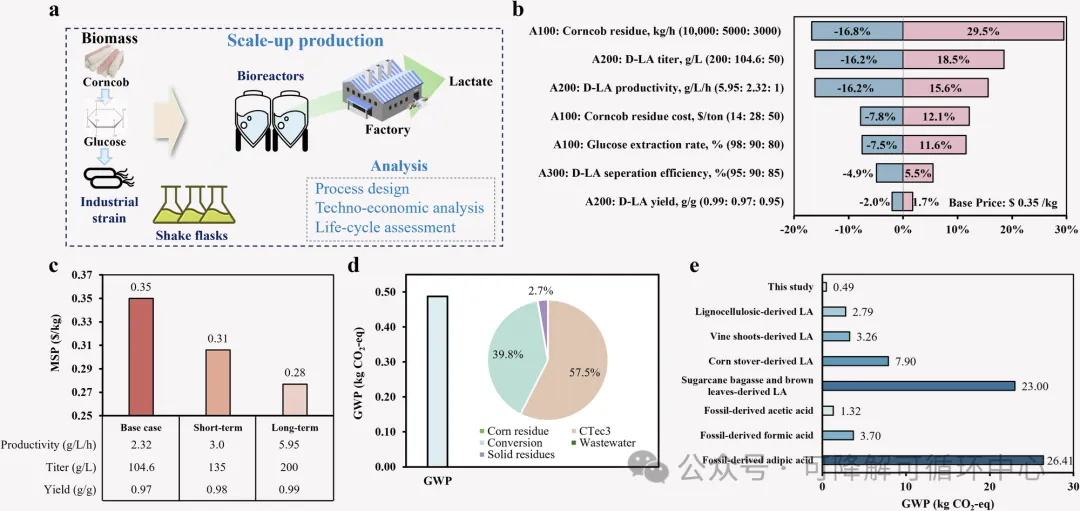
D-乳酸细胞工厂的技术经济分析和生命周期评估
该研究不仅拓宽了运动发酵单胞菌作为优良生物炼制底盘细胞的生产应用范围,也为工程化改造嗜甲烷菌等其他非粮生物利用底盘微生物实现工业性能提供了重要参考和全新策略。

